1. Acilglicéridos
Los acilglicéridos como almacén de energía
Los acilglicéridos son ésteres formados por el alcohol glicerol y ácidos grasos, mediante una
reacción de condensación denominada esterificación.
Cada glicerol puede reaccionar hasta con 3 ácidos grasos, ya que tiene 3 grupos
hidroxilo. Por tanto existen tres grupos:
- Monoacilglicéridos: Cuando el glicerol se esterifica con un solo ácido graso. Se libera una molécula de agua.
- Diacilglicéridos: Glicerol y dos ácidos grasos. Se liberan dos moléculas de agua.
- Triacilglicéridos: El glicerol está unido con tres ácidos grasos, liberándose tres moléculas de agua.
Se puede decir que los
triacilglicéridos son simples si los
tres ácidos grasos son iguales y mixtos
si son diferentes 2 o los 3.
Los triacilglicéridos funcionan como almacén de energía en las células.
Son mucho más eficaces que los hidratos de carbono. Son muy insolubles en agua, ya que al unirse con el glicerol se reduce su potencial hidrófilo.
En los animales, la grasa se
almacena, principalmente, en adipocitos. La mayoría de esta célula está formada
por una gota se grasa. En los seres humanos, el contenido medio de grasa ronda
el 21% en hombres y sobre el 26% en mujeres, lo que les permitiría sobrevivir 2-3
meses a la inanición. Sin embargo, las reservas de glucógeno pueden abastecer
las necesidades de energía durante menos de 1 día. En cuanto a la grasa
subcutánea, proporciona aislamiento térmico, lo que es importante para los
animales acuáticos de sangre caliente. El almacenamiento de grasa en los
animales tiene estas funciones:
- Producción de energía: La mayor parte de grasa se oxida para generar ATP.
- Producción de calor: Algunas células especiales oxidan triacilglicéridos para producir calor.
- Aislamiento: Las capas de células adiposas situadas debajo de la piel actúan como un aislante térmico.
Reacción de saponificación
La saponificación es una reacción química
entre un ácido graso o un lípido saponificable, y una base. Se obtiene como
producto la sal correspondiente.
2. Fosfoglicéridos
Los Fosfoglicéridos, fosfoacilglicéridos o glicerofosfolípidos están
constituidos por dos ácidos grasos (normalmente 1 saturado y 1 insaturado)
esterificados al primer y segundo –OH del glicerol. El tercer grupo está unido
por enlace fosfodiester a un grupo de cabeza muy polar. Todos los fosfoglicéridos
poseen dos colas no polares aportadas por los dos ácidos grasos.
Las cabezas polares se unirán al
grupo fosfato:
Los fosfoglicéridos son lípidos
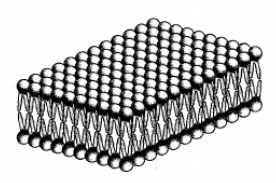
estructurales presentes en las membranas biológicas. Estas membranas están formadas por
una doble capa lipídica que constituye una barrera al paso de moléculas polares
e iones. Los lípidos de membrana son anfipáticos (una parte hidrófoba y otra hidrófila). Las partes hidrófilas se orientan hacia fuera, mientras que las
partes hidrófobas quedan enfrentadas, generando la forma característica de la
membrana. La parte hidrófila está compuesta
por el grupo fosfato y la cabeza polar. La parte hidrófoba está formada por el glicerol y los ácidos grasos.
3. Esfingolípidos
Cuando se une un ácido graso por
enlace amida al –NH2 del C-2 de la esfingosina se obtiene una ceramida. La ceramida es la unidad
estructural fundamental común de todos los esfingolípidos. La siguiente tabla
muestra la molécula que se obtendría si se une una determinada cabeza polar
(representada con una X en la anterior imagen).
Existen varias clases de
esfingolípidos, todos ellos derivados de la ceramida:
- Las esfingomielinas contienen fosfocolina o fosfoetanolamina como grupo de cabeza polar. Se encuentran en las membranas plasmáticas de las células animales y en la vaina de mielina que rodea y aísla los axones de las neuronas mielinizadas.
- Los glucoesfingolípidos se encuentran principalmente en la cara externa de la membrana plasmática. Tienen uno o más azúcares en su grupo de cabeza polar unidos al C-1 de la ceramida (no contienen fosfato). Dentro de este grupo tenemos los cerebrósidos, que tienen un único azúcar unido a la ceramida; los que contienen galactosa se encuentran de manera característica en las membranas plasmáticas de las células del tejido nervioso, mientras que los que contienen glucosa se hallan en las membranas plasmáticas de células de tejidos no nerviosos. Los globósidos son glucoesfingolípidos neutros con dos o más azúcares (normalmente D-glucosa o N-acetil-D-galactosamina). Los gangliósidos son más complejos al contener su cabeza polar formada por oligosacáridos y uno o varios residuos terminales de ácido N-acetilneuramínico (ácido siálico). Este grupo de moléculas se encuentra en el exterior de las células. Sus cabezas de hidratos de carbono actúan como receptores específicos. También son receptores de determinadas toxinas proteicas de origen bacteriano, como la toxina colérica.
4. Ceras: protectores y aislantes
Son ésteres de ácidos grasos de
cadena larga con alcoholes de cadena larga. Sus puntos de fusión son generalmente
más elevados que los de los triacilglicéridos. Las ceras realizan diversas
funciones debido a su hidrofobicidad y consistencia. Por ejemplo, las aves
acuáticas las secretan para mantener la repelencia al agua en sus plumas. Ceras
como la lanolina o la cera de abeja se utilizan en la fabricación de lociones.